蝋梅(ロウバイ)の種子から新しい作用機構をもつ不斉有機触媒を発見―千葉大学天然物ライブラリーの活用と化学的応用―
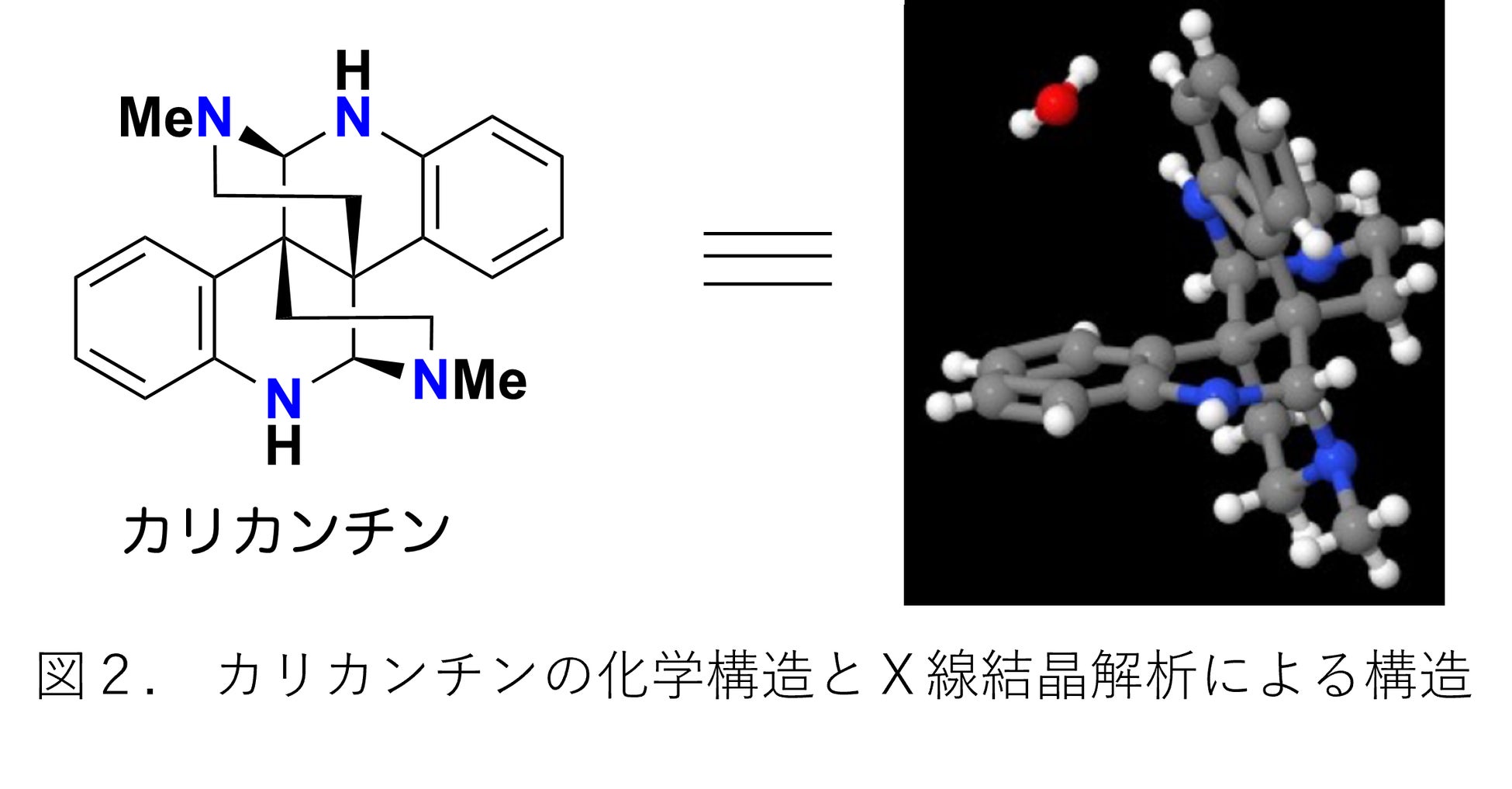
千葉大学大学院医学薬学府博士後期課程3年山西恭輔氏、同大学院薬学研究院原田慎吾准教授および石川勇人教授らの研究グループは、1960年から本学薬学部に蓄積されてきた植物由来アルカロイド(注1)ライブラリーを活用し、医薬品合成などに重要な光学活性分子合成のための有機分子触媒(注2)を探索しました。その結果、日本で園芸品種として親しまれている蝋梅(図1)の種子に大量に含有されている天然有機化合物「カリカンチン(calycathine)」(図2)に、高い触媒活性があることを見出しました。さらに化学合成を駆使し、カリカンチンの触媒活性を高め、医薬品や農薬などの化学合成に有用なマイケル反応(注3)を立体的な特異性(不斉性)を持たせて進行させることに成功しました。
カリカンチンは、抗けいれんや抗真菌、メラニン生成抑制活性などの効果があるとされ、医薬品候補として期待されています。特に、強力な中枢性の抗けいれん作用は注目されていますが、そのメカニズムについては研究段階にあります。本研究成果により、新しい作用機構を有する有機分子触媒が、植物由来天然物の中に存在しているということ、さらに、それらが医農薬などの化学合成に有用であることが示されました。今後の有機化学に新たな潮流が生まれることが期待されます。
この研究成果は2024年9月18日に米化学雑誌Journal of the American Chemical Societyオンライン版にて公開されました。

■研究の背景
有機分子触媒とは、金属元素を含まず、炭素、水素、窒素、酸素などの元素で構成された、比較的分子量の小さい低分子化合物を指します。2000年代に入ってから安価、安全であり、無水、無酸素といった厳密な反応条件を必要としない有機触媒を、光学活性な分子を合成するための不斉反応に応用される研究が、世界中で注目を集めました。現在では、医農薬の合成に積極的に用いられるまでに成長し、2021年にはノーベル化学賞の受賞対象となっています。
これまで開発されてきた不斉有機分子触媒の多くは、人工的に設計、合成されたものです。唯一、マラリアの特効薬であるキナの木から単離されるキニーネが、1900年代初頭から不斉有機触媒として機能することが知られています。しかし歴史的に、植物由来の天然物に関する研究は主に医薬への応用に集中していたため、触媒としての機能評価は行われてきませんでした。
130年以上の歴史を持つ本学薬学部では、1960年ごろから医薬への応用を念頭にした植物由来天然物の収集が行われてきました。現在確認されている約500種のライブラリーのうち、約30%は本学で発見された新規化合物であり、極めて貴重かつ唯一無二のライブラリーです。研究グループは、このライブラリーを医農薬研究へと展開する一方で、天然物のバラエティに富んだ化学構造が新たな触媒機能を生み出す可能性が極めて高いと考え、不斉有機触媒反応としての機能を評価する研究を進めました。
■研究成果1- 天然物ライブラリーから不斉有機触媒の発見
研究グループは、医農薬合成に重要なオキシインドール誘導体(基質1)とニトロスチレン(基質2)を基質とする不斉マイケル反応を利用して、所有する天然物ライブラリーの触媒活性スクリーニングを行いました。その結果、数種の天然物が不斉有機触媒としてある程度機能することを発見し、その中でも蓬莱葛(ホウライカズラ)から単離されるガルドネリン(gardnerine),下野(シモツケ)から単離されるスピラジンA(spiradine A), 蝋梅(ロウバイ)から単離されるカリカンチンの3つの天然物が高い触媒活性を有していることを見出しました(図3)。なお、今回開発した不斉マイケル反応は、一つの炭素に4つの異なる官能基が結合した四級不斉炭素中心を構築できる、医農薬開発に非常に有用な反応と考えられます。

■研究成果2- 天然物の誘導体化による触媒機能の向上
研究成果1で発見した天然物の中から、カリカンチンを選択し、さらに触媒活性を高める検討を行いました。その結果、図4に示すように、カリカンチンのベンゼン環部にヨウ素を導入した人工合成触媒において、非常に高いエナンチオ選択性(注4)で反応が進行することを見出しました(96:4)。収率も90%と非常に高く、実用的な手法に昇華することができました。これまでにカリカンチンに類似する不斉有機触媒は開発されておらず、当研究室の天然物ライブラリーから新しい構造様式をもつ不斉有機触媒を見つけ出すことに成功しました。

■研究成果3- 理論解析による反応メカニズムの解明
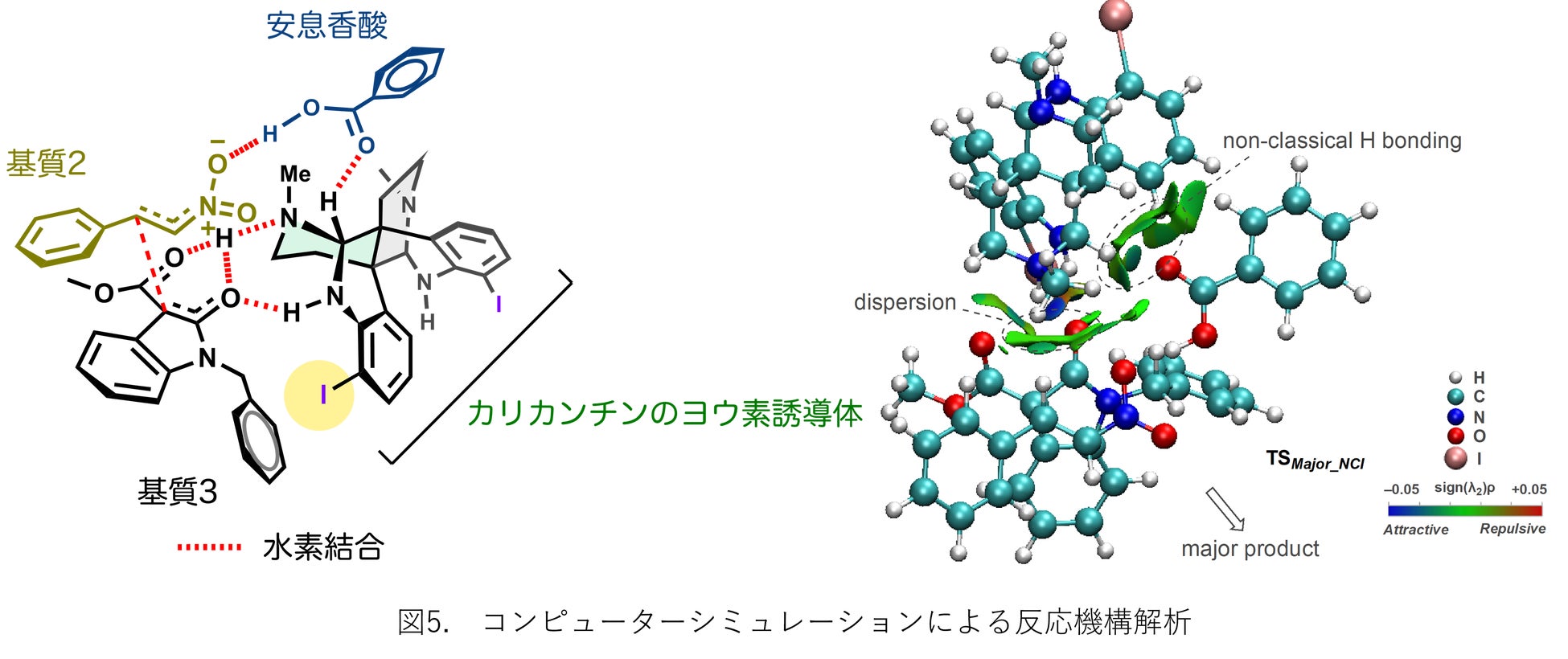
研究グループは計算科学的手法を駆使して、なぜ本反応が極めて高い立体選択性を伴って進行するのかを解明しました。すなわち、DFT計算(注5)を用い、今回開発した触媒のメカニズムを解析しましたところ、成功の鍵となる不斉C-C結合形成(注6)の段階においては、図5のように4つの分子が水素結合ネットワークを形成し不斉環境を構築することで、エナンチオ選択性が制御されていることがわかりました。これらの知見を基盤に、新たな化学反応の設計が期待できることから、その他の不斉C-C結合形成反応の開発や有用物質の合成など他の領域への波及効果も考えられます。
■今後の展望
本研究における新しい科学的なアプローチは、自然界に存在する天然物から有機合成化学において重要な触媒を見出したところにあります。今回は、新しい作用機構を持つ不斉有機触媒を植物の種子から発見しただけではなく、これまで困難であった四級不斉炭素中心を構築する不斉反応であっても、今回見出したカリカンチン型の触媒を使えば、実現可能な場合があると示すことができました。本研究をきっかけに、主に医薬として注目されていた天然物から新しい触媒が次々と見出され、有機分子触媒分野が今後さらに発展することが期待されます。
■研究プロジェクト
本研究は、JST 次世代研究者挑戦的研究プログラム、日本学術振興会 科学研究費助成事業科研費、文部科学省科学研究費助成事業「学術変革研究A:天然物が織り成す化合物潜在空間が拓く生物活性分子デザイン」および「学術変革研究A:デジタル化による高度精密有機合成の新展開」の支援により遂行されました。
■論文情報
論文タイトル:New Entries in Organocatalysts from an Alkaloid Library; Development of Aminal Catalysis for a Michael Reaction Based on Calycanthine
著者: Kyosuke Yamanishi, Gin Ashihara, Shinya Shiomi, Shingo Harada, Mariko Kitajima, Hiromitsu Takayama, and Hayato Ishikawa
雑誌名:Journal of the American Chemical Society
DOI: 10.1021/jacs.4c10242
■用語解説
注1)植物由来アルカロイド:植物に含有されている窒素原子を含む有機化合物。
注2)有機分子触媒:有機反応を触媒する、金属原子を含まない分子。主に炭素、窒素、酸素から成る。
注3)マイケル反応:共役した電子不足二重結合に炭素原子が1,4-付加する反応。
注4)エナンチオ選択的:不斉の要素がない化合物に対して化学反応を行うことで、一方の鏡像異性体が優先的に生成すること。
注5)DFT計算:密度汎関数理論(Density Functional Theory)に基づく計算手法。電子密度やエネルギーなどの分子の物理化学的性質を予測することが可能。
注6)不斉C-C結合形成:有機合成の根幹をなす炭素―炭素結合をエナンチオ選択的に形成すること。
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
